ma. 11 mei 2026

De Amerikaanse FDA heeft een labeluitbreiding goedgekeurd voor Vyvgart en Vyvgart Hytrulo van argenx, waardoor ze nu inzetbaar zijn bij alle subtypes van gegeneraliseerde myasthenia gravis (gMG). Dit betekent dat het middel als eerste en enige behandeling alle serotypes van de ziekte dekt, inclusief moeilijk behandelbare patiëntengroepen. De uitbreiding vergroot het potentiële patiëntenbereik aanzienlijk, aldus KBC Securities-analist Mathijs Geerts Danau.
FDA breidt indicatie uit naar alle gMG-serotypes
argenx kondigde aan dat de Amerikaanse FDA een labeluitbreiding heeft goedgekeurd voor Vyvgart en Vyvgart Hytrulo. De goedkeuring omvat nu alle serotypes van volwassen patiënten met gegeneraliseerde myasthenia gravis, waaronder:
- anti-AChR-Ab positief
- anti-MuSK-Ab positief
- anti-LRP4-Ab positief
- triple seronegatief
Hiermee wordt Vyvgart de enige behandeling die goedgekeurd is voor alle gMG-subtypes. Andere FcRn-remmers zijn momenteel enkel goedgekeurd voor anti-AChR-Ab en anti-MuSK-Ab positieve patiënten en niet voor anti-LRP4-Ab positieve en triple seronegatieve patiënten, die samen ongeveer 10 tot 15 procent van de gMG-populatie vertegenwoordigen.
Klinische data ondersteunen de uitbreiding
De goedkeuring is gebaseerd op de eerder gepubliceerde fase 3-studie ADAPT SERON, die zijn primaire eindpunt behaalde (p=0,0068). Daarin werd aangetoond dat patiënten behandeld met Vyvgart een statistisch significante verbetering van 3,35 punten vertoonden in de MG-ADL-score (Myasthenia Gravis Activities of Daily Living) in vergelijking met placebo na vier weken.
Daarnaast werden verbeteringen in zowel MG-ADL als de Quantitative Myasthenia Gravis (QMG)-score waargenomen over opeenvolgende behandelingscycli. Deze positieve effecten werden vastgesteld in de totale studiepopulatie en in alle onderzochte serotypes.
Het veiligheidsprofiel van Vyvgart bleef consistent met eerdere bevindingen. De behandeling werd goed verdragen over alle serotypes heen, met een veiligheidsprofiel vergelijkbaar met dat bij patiënten met anti-AChR-Ab positieve gMG.
Strategische uitbreiding naar nieuwe patiëntengroepen
Met deze labeluitbreiding wordt een belangrijke onzekerheid weggenomen rond de werkzaamheid bij de triple seronegatieve subgroep. Door deze brede goedkeuring kan Vyvgart nu een bijkomende potentiële populatie van ongeveer 11.000 patiënten in gMG aanspreken.
Bovendien positioneert argenx zich sterk voor een vlotte commerciële lancering. Het bedrijf heeft reeds relaties opgebouwd met meer dan 80 procent van de zorgverleners die seronegatieve gMG behandelen, wat de adoptie in deze nieuwe patiëntengroepen moet vergemakkelijken.
Verdere uitbreiding van het Vyvgart-platform
Naast deze goedkeuring blijft argenx werken aan verdere uitbreidingen van het toepassingsgebied van Vyvgart. Zo werden recent positieve topline-resultaten aangekondigd uit de ADAPT OCULUS-studie in oculaire myasthenia gravis.
Daarnaast plant het bedrijf een uitbreiding van het label naar oculaire MG via een sBLA-indiening, en loopt er momenteel een studie naar pediatrische gMG (ADAPT Jr-studie). Hiermee wil argenx het gebruik van Vyvgart uitbreiden naar alle relevante patiëntengroepen binnen de ziekte.
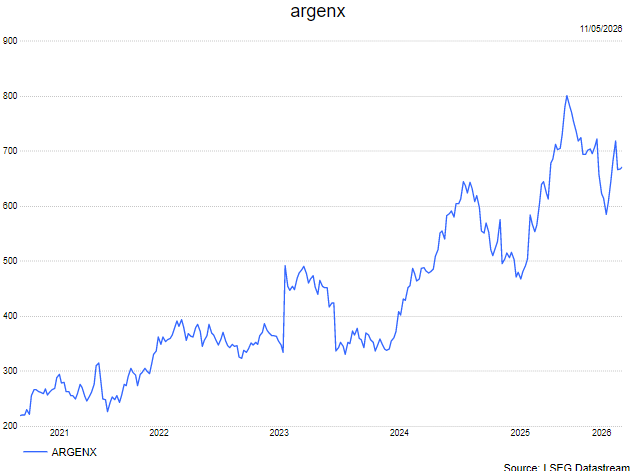
KBC Securities over argenx
Mathijs Geerts Danau stelt dat de timing van de goedkeuring, net voor de PDUFA-datum van 10 mei, belangrijk is en argenx een strategisch voordeel geeft. Hij benadrukt dat Vyvgart nu als enige behandeling alle gMG-serotypes dekt, wat een duidelijke competitieve differentiatie vormt tegenover andere FcRn-remmers.
Volgens de analist worden eerdere vragen rond de effectiviteit bij triple seronegatieve patiënten nu weggewerkt door de brede labeluitbreiding, wat het commerciële potentieel verder vergroot.
Mathijs behoudt zijn kopen-aanbeveling en koersdoel van 900 euro.