di. 7 okt 2025
MaaT: geen veiligheidsproblemen bij fase 2b-studie met microbiomecapsule

Geen veiligheidsproblemen bij MaaT033
De onafhankelijke Data Safety Monitoring Board (DSMB) heeft de tweede geplande veiligheidsanalyse afgerond van de lopende gerandomiseerde fase 2b-studie (PHOEBUS, NCT05762211) met MaaT033, een orale microbiomecapsule. Deze therapie is bedoeld voor patiënten die een allogene hematopoëtische stamceltransplantatie (allo-HSCT) ondergaan.
De DSMB bekeek niet-geblindeerde veiligheidsdata van 120 patiënten, waarvan 60 werden behandeld met MaaT033. De patiënten werden gedurende 90 dagen na hun transplantatie opgevolgd, zoals voorgeschreven in het studieprotocol. Naast deze specifieke analyse voert de DSMB ook routineveiligheidsbeoordelingen uit om de zes maanden.
Op basis van de huidige gegevens stelde de DSMB geen veiligheidsproblemen of overmatige sterfte vast die verband houden met MaaT033. De commissie gaf dan ook groen licht om de studie verder te zetten zoals gepland.
Internationale studie met commerciële ambitie
De patiëntenwerving voor de PHOEBUS-studie is nog aan de gang in Frankrijk, Duitsland, België, Spanje, Nederland en het Verenigd Koninkrijk. In totaal zullen 387 patiënten worden opgenomen in de studie, die zal plaatsvinden op maximaal 60 locaties.
De volgende routineveiligheidsanalyse door de DSMB wordt verwacht in het eerste kwartaal van 2026. De toplijnresultaten over werkzaamheid worden voorzien in de tweede helft van 2027.
Volgens Jakob Mekhael is MaaT033 het volgende product in de pijplijn van MaaT, en onderscheidt het zich van het leidende product MaaT013 door zijn orale toedieningsvorm (capsule in plaats van een klysma). Dit maakt het mogelijk om een bredere patiëntenpopulatie te bereiken binnen allo-HSCT, wat gepaard gaat met een groter commercieel potentieel. Noyens schat de piekverkoop van MaaT033 op ongeveer 400 miljoen euro.
Breder klinisch programma met MaaT013
Op kortere termijn kijkt Jakob uit naar de fase 2a-resultaten van de PICASSO-studie, een door onderzoekers geïnitieerde fase 2-studie met MaaT013 in combinatie met immuuncheckpointremmers bij metastatische melanoom. Deze resultaten worden verwacht in de tweede helft van 2025 en zouden MaaT’s bereik in solide tumoren kunnen uitbreiden.
Daarnaast worden tegen het einde van 2025 de volledige overlevingsdata (OS) verwacht van de fase 3-studie met MaaT013 bij acute graft-versus-host disease (aGvHD).
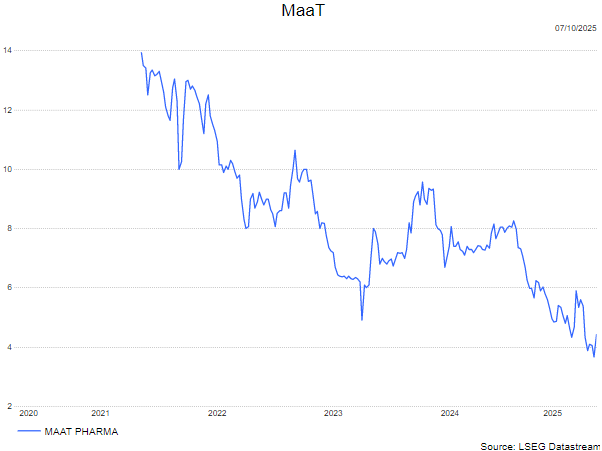
KBC Securities over MaaT Pharma
Jakob blijft positief over MaaT. Hij benadrukt dat de veiligheidsdata van MaaT033 een belangrijke mijlpaal zijn in het klinisch programma van het bedrijf. De bredere toepasbaarheid van de orale capsule en de aankomende data van MaaT013 versterken volgens hem het potentieel van MaaT in zowel hematologische als solide indicaties.
Jakob handhaaft zijn kopen-aanbeveling en stelt het koersdoel op 17 euro.









